
Ламитор 50 мг таблетки 30 шт для лечения эпилепсии и биполярного расстройства
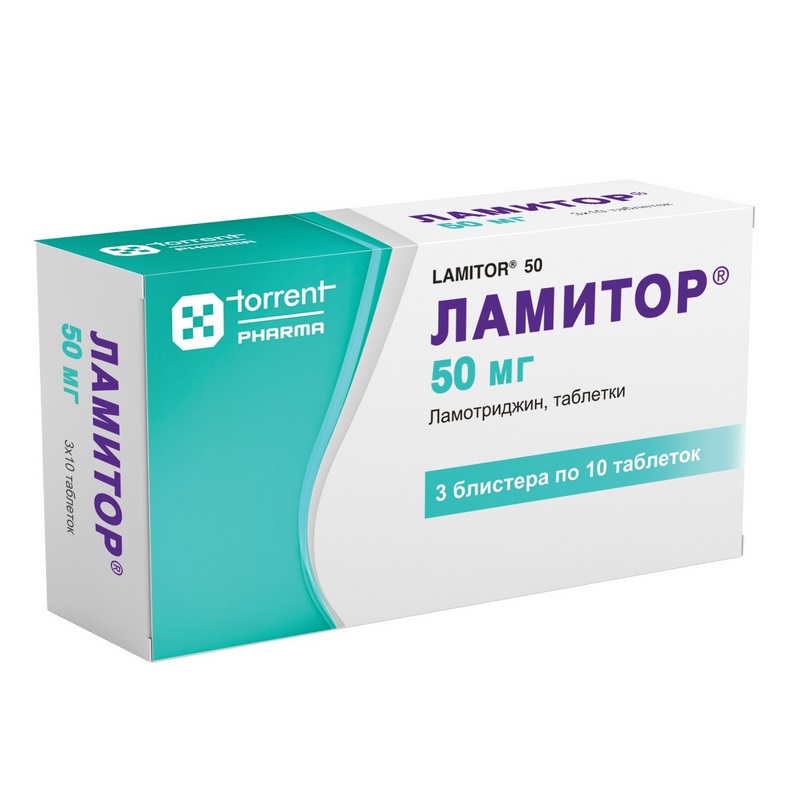

Источник изображений товара: Аптека Озерки. Внешний вид товара может отличаться от изображённого
- Бренд:
- Производитель:
- Модель:

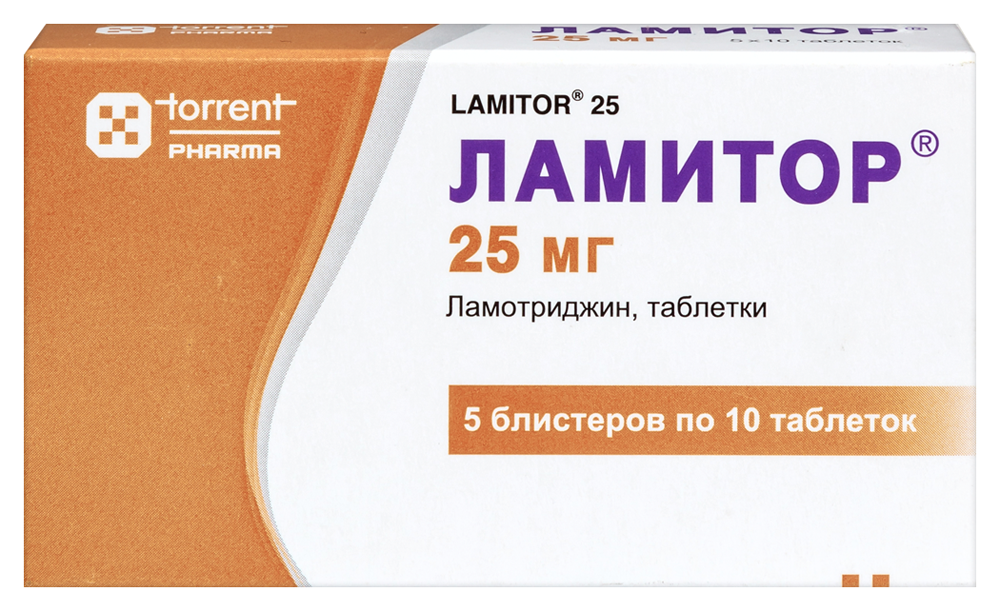
Ламитор 25 мг 50 шт. таблетки для лечения эпилепсии и биполярного расстройства

Ламитор таблетки 50 мг 30 шт противоэпилептическое средство

ЛАМИТОР табл. 50 мг №30
Ламитор таблетки 50мг 30 шт лечение эпилепсии и биполярного расстройства
Ламитор таблетки 50мг №50 - противосудорожное средство

Ламитор таблетки 50 мг 30 шт - лечение эпилепсии и нейропатической боли
Информация носит справочный характер и не является руководством к применению. Обязательна консультация врача.
Ламитор 50 мг таблетки - эффективное противоэпилептическое средство, широко применяемое для лечения эпилепсии и биполярного расстройства. В состав входит ламотриджин, который способствует стабилизации нейронной активности и предотвращению судорожных припадков. Препарат подходит для взрослых и детей старше 3 лет, его можно использовать как в монотерапии, так и в составе комбинированной терапии. Ламитор обладает быстрым и полным всасыванием после перорального приема, а его фармакокинетика зависит от уровня функции печени, почек и сопутствующих препаратов. Он показан при парциальных и генерализованных припадках, а также для профилактики нарушений настроения при биполярном расстройстве. Средняя доза для взрослых и детей подбирается индивидуально в зависимости от характера заболевания и реакции организма, что делает препарат универсальным решением для разных пациентов. Преимущества включают высокую эффективность, хорошую переносимость и возможность применения в составе комплексной терапии без значимых взаимодействий с другими ЛС.
- Артикул магазина
- 113696
- Бренд
- Ламитор
- Дозировка
- 50 мг
- Количество
- 30 шт
- Показания
- Эпилепсия, биполярное расстройство
- Форма выпуска
- Таблетки
- Классификация
- Фенилтриазины
- Фармакокинетика
- Наука о движении лекарства по организму
- Понимание T1/2
- Время, за которое концентрация препарата уменьшается вдвое
- Клиренс
- Объем крови, очищенный от препарата за единицу времени
- Взаимодействия
- Влияние препарата на эффективность других лекарств
- Метаболизм
- Преобразование лекарства в организме
Сравнение товаров
| Бренд | ||||
| Ламитор | Торрент Фармасьютикалс | — | Торрент Фармасьютикалс | Акрихин |
| Дозировка | ||||
| 50 мг | — | 500 мг | 100 мг | 50 мг |
| Количество | ||||
| 30 шт | — | — | 30 таблеток | 30 шт |




